Chlorid zlatitý
| Chlorid zlatitý | |
|---|---|
 Roztok | |
 Strukturní vzorec | |
 3D vzorec | |
| Obecné | |
| Systematický název | Chlorid zlatitý |
| Anglický název | Gold(III) chloride |
| Německý název | Gold(III)-chlorid |
| Sumární vzorec | AuCl3, Au2Cl6 (dimer) |
| Vzhled | Červená hygroskopická pevná látka |
| Identifikace | |
| Registrační číslo CAS | 13453-07-1 |
| Číslo RTECS | MD5420000 |
| Vlastnosti | |
| Molární hmotnost | 303,326 g/mol |
| Teplota tání | 288 °C (od 185 °C pozvolný rozklad) |
| Teplota sublimace | 265 °C |
| Hustota | 4,67 g/cm3 |
| Rozpustnost ve vodě | 68 g/100 g |
| Měrná magnetická susceptibilita | 4,65×10−6cm3g−1 |
| Struktura | |
| Krystalová struktura | jednoklonná |
| Koordinační geometrie | čtvercově rovinná |
| Termodynamické vlastnosti | |
| Standardní slučovací entalpie ΔHf° | −118,4 kJ/mol |
| Standardní molární entropie S° | 164,4 JK−1mol−1 |
| Standardní slučovací Gibbsova energie ΔGf° | −53,6 kJ/mol |
| Bezpečnost | |
 GHS05  GHS07 Nebezpečí[1] | |
| R-věty | R34, R36/37/38 |
| S-věty | S26, S36, S36/37/39 |
Některá data mohou pocházet z datové položky. | |
Chlorid zlatitý (chemický vzorec AuCl3) je nejběžnější sloučeninou zlata. Z českého chemického názvosloví vyplývá, že je zlato v této sloučenině v oxidačním čísle III+. Existují ještě dvě sloučeniny zlata s chlorem, chlorid zlatný a kyselina chlorozlatitá.
Příprava
Chlorid zlatitý se nejčastěji připravuje přímou chlorací čistého zlata za vysokých teplot:
- 2 Au + 3 Cl2 → 2 AuCl3
Vlastnosti
Bezvodý chlorid zlatitý se již za teploty okolo 160 °C rozkládá v chlorid zlatný. Touto reakcí se dá připravovat čisté zlato, protože chlorid zlatný se následně za teploty okolo 420 °C rozkládá na zlato a zpět na chlorid zlatitý (dochází k disproporcionaci):
- AuCl3 → AuCl + Cl2
- 3 AuCl → AuCl3 + 2 Au
Reakcí s vodným roztokem kyseliny chlorovodíkové vzniká komplexní sloučenina nazývaná kyselina chlorozlatitá:[2]
- HCl (aq) + AuCl3 (aq) → HAuCl4 (aq)
Obdobně probíhá reakce chloridu zlatitého s chloridy, produktem jsou poté příslušné chlorozlatitany.
Struktura molekuly
Chlorid zlatitý existuje, podobně jako bromid zlatitý, jako dimer. To znamená, že jeho molekula vypadá takto:
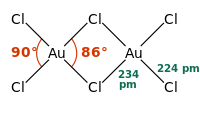
Použití
Chlorid zlatitý je nejběžnější chemickou sloučeninou zlata, pro přípravu ostatních sloučenin zlata bývá výchozí látkou. Připravuje se z něj např. komplexní sloučenina tetrakyanozlatitan draselný:
Chlorozlatité soli, hlavně tetrachlorozlatitan sodný, vznikající reakcí chloridu zlatitého a chloridu sodného, se používají jako katalyzátor při reakcích.
Ve fotografii se používá jako tónovací lázeň.
Odkazy
Reference
Související články
- chlorid zlatný
- kyselina chlorozlatitá
- bromid zlatitý
Externí odkazy
 Obrázky, zvuky či videa k tématu chlorid zlatitý na Wikimedia Commons
Obrázky, zvuky či videa k tématu chlorid zlatitý na Wikimedia Commons
Literatura
- VOHLÍDAL, JIŘÍ; ŠTULÍK, KAREL; JULÁK, ALOIS. Chemické a analytické tabulky. 1. vyd. Praha: Grada Publishing, 1999. ISBN 80-7169-855-5.
| Chloridy s prvkem v oxidačním čísle III. | |
|---|---|
| Chlorid hlinitý (AlCl3) • Chlorid antimonitý (SbCl3) • Chlorid arsenitý (AsCl3) • Chlorid boritý (BCl3) • Chlorid bismutitý (BiCl3) • Chlorid ceritý (CeCl3) • Chlorid chromitý (CrCl3) • Chlorid erbitý (ErCl3) • Chlorid europitý (EuCl3) • Chlorid gadolinitý (GdCl3) • Chlorid gallitý (GaCl3) • Chlorid holmitý (HoCl3) • Chlorid inditý (InCl3) • Chlorid iriditý (IrCl3) • Chlorid železitý (FeCl3) • Chlorid lanthanitý (LaCl3) • Chlorid lutecitý (LuCl3) • Chlorid neodymitý (NdCl3) • Chlorid niklitý (NiCl3) • Chlorid niobitý (NbCl3) • Chlorid joditý (I2Cl6) • Chlorid dusitý (NCl3) • Chlorid fosforitý (PCl3) • Chlorid promethitý (PmCl3) • Chlorid praseodymitý (PrCl3) • Chlorid plutonitý (PuCl3) • Chlorid rhoditý (RhCl3) • Chlorid rhenitý (ReCl3) • Chlorid ruthenitý (RuCl3) • Chlorid samaritý (SmCl3) • Chlorid skanditý (ScCl3) • Chlorid terbitý (TbCl3) • Chlorid thallitý (TlCl3) • Chlorid thulitý (TmCl3) • Chlorid titanitý (TiCl3) • Chlorid uranitý (UCl3) • Chlorid wolframitý (WCl3) • Chlorid vanaditý (VCl3) • Chlorid ytterbitý (YbCl3) • Chlorid yttritý (YCl3) • Chlorid zlatitý (AuCl3) • Chlorid zirkonitý (ZrCl3) • Chlorid americitý (AmCl3) • Chlorid kobaltitý (CoCl3) | |










